乳癌は女性のがん発生率の第1位を占めるようになり,国民の乳癌への関心は年々高くなってきた。 乳癌に対する手術治療も大きく変化しており,乳房周囲の組織を含めて患部を根こそぎ切除するとい った手術法から,乳房皮膚を温存して乳腺だけを切除するSkin-sparing mastectomyや,乳癌を含 む乳腺組織を部分的に切除する温存手術へと縮小化が図られている。しかし,乳癌手術の縮小化により術後の乳房形態が飛躍的に改善したとは言い難く,乳房温存手術といえども乳癌の部位によっては乳房形態の高度変形を来すことが多いのが現状である。
そのような状況下,乳癌術後の乳房再建術が最近脚光を浴びるようになり,乳癌患者からの再建の要求も増えてきた。さまざまな乳癌手術後の多様な変形に対応した乳房再建術が必要であり,近年欧米はもとより本邦でも多くの報告が認められる。
従来から行われてきたオーソドックスな再建方法としては,腹直筋皮弁法,広背筋皮弁法,インプラント法などがある。また最近注目されている方法としては,筋肉を犠牲にしない穿通枝皮弁法がある。さらに,本邦でも脂肪注入や真皮脂肪移植といった再建術式が発表されているが,成績が一定しないため議論を巻き起こしている。
一方,再建手術に関して影響を与える患者側要因として,放射線治療,化学療法,肥満,喫煙,高齢などが挙げられる。このような種々の要因を考慮して再建術式を選択することはいうまでもない。
多くの再建術式や手術に影響を与える要因にはさまざまな問題点があるが,標準化の視点から検討を加え,また,今後の解決すべき問題点を抽出すべく,ここにガイドラインとしてまとめた次第である。
1.診療ガイドライン作成の目的と注意点
本ガイドラインは,形成外科が関わる疾患を対象とし,医療者と患者が特定の臨床状況で適切な判断を下せることを支援する目的で作成するものである。
したがって,ガイドラインの根拠にかかる情報収集(文献検索・検討)においては,「研究デザインによる視点」のみならず「臨床的意義による視点」を重視し,形成外科診療の実情を反映したものとする。
なお,本ガイドラインは,現在得られるエビデンスを集積・整理・検討し,現時点での一般診療に有用な情報提供を目的とするものであり,個別の診療(診断法,治療法)を制限するものではない。また,今後行われる(または現在進行中の)臨床研究の成果により内容が大きく変更される可能性がある。
2.作成主体
本ガイドラインは,三学会合同ガイドライン委員会が作成した原案に日本形成外科学会ガイドライン作成部会ならびに日本創傷外科学会ガイドライン作成委員会,日本頭蓋顎顔面外科学会ガイドライン作成委員会が吟味を加え,パブリックコメントを得たうえで公表するものである。
なお,本ガイドラインの内容については学会が責任を負うが,個々の患者の診療結果に関する直接の責任は治療を担当した医師,病院等に帰属すべきものである。また,保険医療の審査基準や医事紛争・医療訴訟の資料として用いることは,本ガイドラインの趣旨から逸脱することは言うまでもない。
3.作成の原則
EBM の手法に基づいて作成することを原則とした。
4.ガイドラインの対象
本ガイドラインは医師および関係する医療者を対象とした。
5.文献検索の範囲
形成外科疾患ガイドラインに用いた文献検索の範囲は,以下に示す①の範囲であるが,必要に応じて,②の範疇にあるものを加えた。
- ①MEDLINE,医学中央雑誌およびCochrane library で検索した臨床研究のメタアナリシス,の臨床研究に関する文献。
- ②上記以外の診療ガイドライン,総説,専門的見地からの意見,成書。
なお,非臨床研究に関する文献で参考となる重要な資料がある場合には引用してもよいが,推奨度
決定の判断には含めない(表2 注2 参照)。
6.文献検索期間
1982 年以降2010~11 年12 月(ガイドラインの作成開始日が項目によって異なるため)に公表されたものを検索の対象とした。文献検索期間がこれと異なるCQ では,該当するCQ で文献検索期間を別に記載した。
7.エビデンスレベル
エビデンスレベルは,研究デザインによる科学的妥当性を根拠とした(表1)。
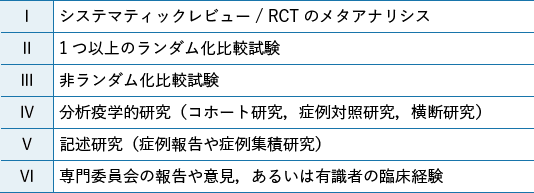
- 注)
- 個々のCQ に関して複数のエビデンスレベルがある場合には,原則として内容を吟味したうえで上記表に準じたレベルの高いエビデンスを採用した。また,どうしても判断がつかない論文については,その判断をプロに依頼した。
8.推奨度について
推奨度(表2)とは,あくまで臨床研究ならびに疫学研究などの文献から得られた情報を根拠とするものである。まず,①エビデンスレベル,②同じ結論に至るエビデンスの多さ,ばらつきの少なさ,③臨床的有効性の大きさ,④臨床上の適用性の広さ,⑤合併症の少なさ,⑥医療コストの多寡の順で検討し,さらに,総合的評価を加え決定した。
なお,本ガイドラインでは,形成外科臨床の実情をガイドラインに反映させるため,エビデンスが乏しい場合の推奨度の決定に関しては,以下の見解を参考とし,ガイドライン委員会のコンセンサスを最終判断の基準とした(表2 注3 参照)。
Canadian Task Force on Preventing Health Care. Decision Making When Evidence is Uncleare;
http:www.ctfphc.org/ctfphc&methods.htm(現在はリンク使用不可)

- 注1)
- 保険適用外もしくはその可能性があるものには(*)を付記した。
- 注2)
- 非臨床研究(作用機序を証明するような基礎実験,臨床症例の効果を裏付ける基礎研究などを含む)の文献を引用する場合には,文献欄の末尾に[非臨床研究]の旨を付記した。
- 注3)
- 表2 の括弧内に記載したエビデンスレベルは推奨度決定の際の目安を示すものである。文献的知見が不足しているものであって,表2 によると推奨度に問題が生じる場合等では,形成外科臨床の実情を勘案し,ガイドライン作成班およびガイドライン作成委員会の吟味,さらにはパブリックコメントを踏まえ,推奨度を決定した。また,エビデンスが少なく,今後の臨床研究の必要性が求められる項目については,その旨をガイドライン中に「今後の課題」として記載した。
9.改訂
ガイドラインの内容は,診療状況の進歩・変化を勘案し,5 年を目途に改訂を予定する。
10.作成に係る資金源について
本ガイドライン作成に係る資金は,内容の公平性を左右するような民間企業等からの支援を受けたものではない。また,本ガイドラインにおける勧告内容および作成に携わった委員,協力委員等は,特定の団体や製品・技術等との利害関係を有するものではなく,委員相互にも利害対立はない。
以上のことは,作成に携わったメンバーからの利益相反申告書により確認した。
